Enews128 淺談骨組織再生
出自KMU e-News
| 第8行: | 第8行: | ||
醫藥暨應用化學系 王志光助理教授 | 醫藥暨應用化學系 王志光助理教授 | ||
| + | |||
| + | [[Image:enews128專題-1.jpg|400px]] | ||
| + | |||
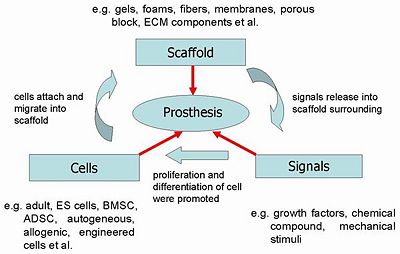
| + | 圖、組織工程三要素(Tissue Engineering Triad)及其內涵成份。 | ||
骨折是外傷中重要的事件,美國每年花費於骨折之治療約4億美元。較大之骨缺損是醫療上的一大挑戰,若使用骨移植(bone graft)填充骨缺損部位可以達到骨傳導(osteo-conduction)及骨誘導(osteo-induction)之雙重效果,但無論自體或異體骨移植來源均很短缺。目前的理論認為理想的骨組織再生應使用具骨傳導之生物材料(biomaterial)、具骨誘導之生長因子(growth factor)及具造骨能力之細胞 (osteogenic cells),如圖1所示之組織工程三要素。已市售之生物材料主要是生物高分子(biopolymer; 例如 PLA, PGA, PLGA, collagen 等)、磷酸鈣、hydroxyapatite (HAp)及硫酸鈣(calcium sulfate)等。生物高分子雖具生物降解性(bio-degradable)但卻無法抗機械力;HAp可抗機械力但一般認為其降解速度太慢;硫酸鈣則是降解速度太快之疑慮。 | 骨折是外傷中重要的事件,美國每年花費於骨折之治療約4億美元。較大之骨缺損是醫療上的一大挑戰,若使用骨移植(bone graft)填充骨缺損部位可以達到骨傳導(osteo-conduction)及骨誘導(osteo-induction)之雙重效果,但無論自體或異體骨移植來源均很短缺。目前的理論認為理想的骨組織再生應使用具骨傳導之生物材料(biomaterial)、具骨誘導之生長因子(growth factor)及具造骨能力之細胞 (osteogenic cells),如圖1所示之組織工程三要素。已市售之生物材料主要是生物高分子(biopolymer; 例如 PLA, PGA, PLGA, collagen 等)、磷酸鈣、hydroxyapatite (HAp)及硫酸鈣(calcium sulfate)等。生物高分子雖具生物降解性(bio-degradable)但卻無法抗機械力;HAp可抗機械力但一般認為其降解速度太慢;硫酸鈣則是降解速度太快之疑慮。 | ||
| 第14行: | 第18行: | ||
更進一步為了加速骨癒合時效,促骨生長因子藥物的添加亦是近年來嶄新的研究方向。例如在2004年時,醫材大廠Medtronic公司應用rhBMP-2 (Bone Morphogenetic Protein-2;骨骼成形基因蛋白質) 發展出INFUSER骨替代物,此產品為結合rhBMP-2與膠原蛋白載體做為脊椎手術後加速脊椎融合的骨材。然而許多文獻針對此類之產品進行長期術後追蹤後發現疑似因生長因子的劑量過多造成發炎及贅骨壓迫神經之併發症等問題尚待克服( McIntyre, Deer & Hayek, 2007;Shields et al., 2006; Carreon et al., 2008)。因此研發一種兼具骨傳導、骨誘導、穩定降解以及控制釋放促骨生成藥物之骨材,並且在臨床上無不良副作用、使用方便、製造簡單及價格低廉等優勢是此類組織工程發展的方向。 | 更進一步為了加速骨癒合時效,促骨生長因子藥物的添加亦是近年來嶄新的研究方向。例如在2004年時,醫材大廠Medtronic公司應用rhBMP-2 (Bone Morphogenetic Protein-2;骨骼成形基因蛋白質) 發展出INFUSER骨替代物,此產品為結合rhBMP-2與膠原蛋白載體做為脊椎手術後加速脊椎融合的骨材。然而許多文獻針對此類之產品進行長期術後追蹤後發現疑似因生長因子的劑量過多造成發炎及贅骨壓迫神經之併發症等問題尚待克服( McIntyre, Deer & Hayek, 2007;Shields et al., 2006; Carreon et al., 2008)。因此研發一種兼具骨傳導、骨誘導、穩定降解以及控制釋放促骨生成藥物之骨材,並且在臨床上無不良副作用、使用方便、製造簡單及價格低廉等優勢是此類組織工程發展的方向。 | ||
| - | |||
| - | |||
| - | |||
| - | 圖、組織工程三要素(Tissue Engineering Triad)及其內涵成份。 | ||
| - | |||
在2009年3月13日 (五) 17:33所做的修訂版本
高雄醫學大學e快報 第128期 生命科學院 專題
淺談骨組織再生
醫藥暨應用化學系 王志光助理教授
圖、組織工程三要素(Tissue Engineering Triad)及其內涵成份。
骨折是外傷中重要的事件,美國每年花費於骨折之治療約4億美元。較大之骨缺損是醫療上的一大挑戰,若使用骨移植(bone graft)填充骨缺損部位可以達到骨傳導(osteo-conduction)及骨誘導(osteo-induction)之雙重效果,但無論自體或異體骨移植來源均很短缺。目前的理論認為理想的骨組織再生應使用具骨傳導之生物材料(biomaterial)、具骨誘導之生長因子(growth factor)及具造骨能力之細胞 (osteogenic cells),如圖1所示之組織工程三要素。已市售之生物材料主要是生物高分子(biopolymer; 例如 PLA, PGA, PLGA, collagen 等)、磷酸鈣、hydroxyapatite (HAp)及硫酸鈣(calcium sulfate)等。生物高分子雖具生物降解性(bio-degradable)但卻無法抗機械力;HAp可抗機械力但一般認為其降解速度太慢;硫酸鈣則是降解速度太快之疑慮。
無論如何,具骨傳導之骨材,例如硫酸鈣(calcium sulfate)及氫氧基磷灰石 (HAp)等,在骨移植方面,已有相當多的學者進行新製程開發,以及體外測試等研究。在美國及歐洲地區,亦有廠商陸續推出市售商品,例如OsteoSet®, Calforma®供臨床使用。近來許多研究指出此類合成骨材,除了有利引導骨細胞移入骨材功能外,學者認為骨材的表面積、材質孔隙率及晶體之粒徑尺寸,皆可能為影響骨新生的關鍵因素(Thierry et al.,1999,Gauthier et al., 1998,Madihally & Matthew, 1999,Kong et al,. 2007)。例如早期Hench (1987)等學者認為骨材孔洞直徑之最小要求為100μm,而大於200μm是造成骨新生效應的主要因素。Fabbi (1995)等學者則認為當骨填充物之孔隙度大於150μm時,雖然機械強度會降低,但對於臨床上的使用要求已足夠。近期Kong et al., (2007) 在Journal of Biomaterials Applications期刊中指出, 100-350μm有利於骨組織的生長。故具適當孔隙是目前使用之骨材之必要條件。
更進一步為了加速骨癒合時效,促骨生長因子藥物的添加亦是近年來嶄新的研究方向。例如在2004年時,醫材大廠Medtronic公司應用rhBMP-2 (Bone Morphogenetic Protein-2;骨骼成形基因蛋白質) 發展出INFUSER骨替代物,此產品為結合rhBMP-2與膠原蛋白載體做為脊椎手術後加速脊椎融合的骨材。然而許多文獻針對此類之產品進行長期術後追蹤後發現疑似因生長因子的劑量過多造成發炎及贅骨壓迫神經之併發症等問題尚待克服( McIntyre, Deer & Hayek, 2007;Shields et al., 2006; Carreon et al., 2008)。因此研發一種兼具骨傳導、骨誘導、穩定降解以及控制釋放促骨生成藥物之骨材,並且在臨床上無不良副作用、使用方便、製造簡單及價格低廉等優勢是此類組織工程發展的方向。